W 2022 roku znowelizowano ustawę o przeciwdziałaniu narkomanii, wprowadzając art. 49a i otwierając instytutom badawczym drogę do legalnej uprawy konopi innych niż włókniste (konopi medycznych) na potrzeby wytwarzania surowca farmaceutycznego. Kilka lat później wciąż jednak nie doczekaliśmy się na rynku polskiej medycznej marihuany z krajowej uprawy, choć właśnie to miało być jednym z najważniejszych efektów tej zmiany.
Od 3 lat pracuję w sektorze medycznych konopi w Polsce, gdzie pełnię rolę interim dyrektora ds. jakości. W poniższym artykule chciałbym się podzielić perspektywą z pierwszej osoby o tym jak przepisy te wpłynęły na rynek i dlaczego według mojej subiektywnej analizy dzisiaj wciąż nie mamy polskiego surowca farmaceutycznego polskiej produkcji w aptekach, pomimo wielu już zapowiedzi, że niebawem ten surowiec pojawi się w aptekach albo, że już ruszyły uprawy surowca, który do tych aptek trafi, co moim skromnym zdaniem nie jest prawdą.
Na potrzeby tego artykułu ważna wstawka. Według ustawy o przeciwdziałaniu narkomanii nie istnieje coś takiego jak konopie medyczne, prawidłowym terminem, którym należy posługiwać się dla tego typu produktu leczniczego jest konopia inna niż włóknista (czyli taka, która zawiera powyżej 0,3% THC). Na potrzeby tego tekstu (oraz SEO :)) tymi terminami będę posługiwał się zamiennie.
1. Instytuty badawcze jako jedyny dopuszczony podmiot
Sam pomysł, aby uprawę konopi innych niż włókniste na potrzeby farmaceutyczne powierzyć instytutom badawczym, nie był z natury zły. Rozumiem logikę tego rozwiązania. Ustawodawca chciał zacząć ostrożnie, zachować większą kontrolę nad nowym segmentem rynku i oprzeć go na podmiotach, które z definicji powinny mieć zaplecze organizacyjne, naukowe i publiczny nadzór. Na papierze wyglądało to rozsądnie, jeśli uwzględnimy popyt społeczeństwa na medyczną marihuanę i to, że jest to środek jest kwalifikowany jako odurzający.
Problem pojawił się dopiero wtedy, gdy ten model trzeba było uruchomić w praktyce. Instytut badawczy nie działa jak prywatna spółka budowana od początku pod jeden cel technologiczny. Instytuty mają swoje ograniczenia budżetowe, organizacyjne, inwestycyjne i kadrowe. Może mieć kompetencje naukowe, ale to nie oznacza jeszcze, że mają zdolność do szybkiego zbudowania przemysłowej uprawy indoor, utrzymywanej w reżimie jakościowym i bezpieczeństwa właściwym dla materiału, który ma finalnie trafić do pacjenta.
Tu dochodzimy do pierwszej realnej bariery. Uprawa tego typu nie ma ekonomicznego sensu w bardzo małej skali. Jeżeli podmiot buduje obiekt, zatrudnia personel, tworzy zabezpieczenia, utrzymuje osobę wykwalifikowaną wymaganą ustawą, finansuje energię, media, laboratoria, serwis i nadzór jakości, to robienie tego dla produkcji rzędu około 200 kilogramów rocznie nie daje zdrowej ekonomii. Taka skala nie wysyci rynku, a koszty stałe pozostaną ogromne. Uprawa konopi medycznych to biznes jak każdy inny w kontekście dostarczania leku na rynek, dlatego musi się również opłacać. W dodatku produkcja w postaci 200 kg byłaby bardziej postrzegana jako marginalne wysycenie rynku (może nawet jako produkt kolekcjonerski), kiedy limity w 2025 roku wynosił 20 ton. W praktyce więc instytut realnie powinien „wejść” w inwestycję większą, droższą i bardziej ryzykowną, niż wynikałoby to z samej litery ustawy.
Druga bariera jest mniej oczywista, ale równie ważna. Artykuł 49a ustawy określa ramę formalną, natomiast nie opisuje wszystkiego, co w realnym świecie trzeba wdrożyć, żeby materiał z uprawy miał szansę przejść dalej. I tu wchodzą wymagania jakościowe, które wprost z przepisu nie wynikają (nie jest opisane w jakim zakresie należy wdrożyć system jakości), ale pośrednio są nieuniknione. Jeżeli ktoś chce produkować materiał, który ma mieć jakość farmaceutyczną, to sama legalność uprawy nie wystarczy. Trzeba wdrożyć system jakości taki jak GACP, czyli Dobrej Praktyki Uprawy i Zbioru. To oznacza higienę personelu, nadzór nad materiałem rozmnożeniowym, dokumentowanie warunków uprawy, kontrolę dostawców, szkolenia, identyfikację partii, zapisy z procesu, nadzór nad zmianami i pełną odtwarzalność tego, co wydarzyło się z rośliną od pierwszego dnia.
Dlatego od początku uważałem, że największym problemem nie było samo dopuszczenie instytutów, tylko to, że wybrano model ostrożny prawnie, ale bardzo trudny operacyjnie. Już w trakcie prac parlamentarnych było widać, że to rozwiązanie będzie wymagało czegoś więcej niż samego przepisu. I dokładnie tak się stało.
2. Zawiłości prawne, czyli kto właściwie ma co robić
W teorii można powiedzieć: dobrze, instytut może uprawiać, więc sprawa rusza. W praktyce to dopiero początek. Bo zaraz pojawia się pytanie, które przez długi czas wcale nie było tak oczywiste, jak dziś może się wydawać: kto po uprawie przejmuje materiał i w jakim reżimie to jego przetwarzanie dalej się odbywa?
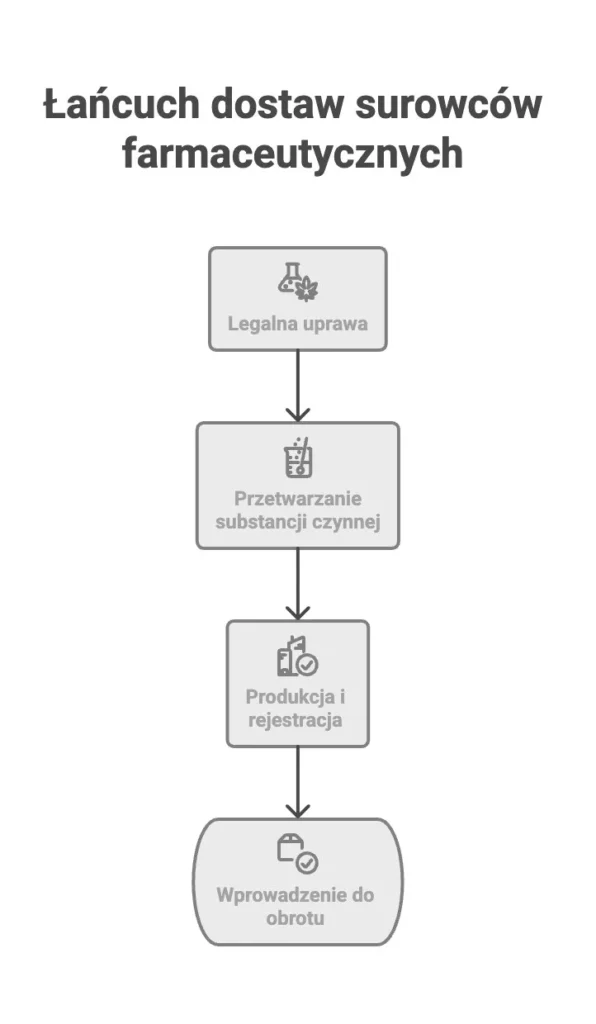
Dziś najbardziej logiczny porządek wygląda następująco: instytut prowadzi legalną uprawę, następnie materiał trafia do podmiotu działającego na poziomie substancji czynnej, a dopiero później do podmiotu, który wytwarza i rejestruje surowiec farmaceutyczny dopuszczany do obrotu. Problem polega na tym, że dojście do takiego uporządkowania zajęło czas, a nawet po jego wypracowaniu okazało się, że w Polsce praktycznie nie wykształcił się segment wytwórców gotowych wejść w etap substancji czynnej dla konopi innych niż włókniste.
To nie wynikało z braku teorii, tylko z braku opłacalności. Na wczesnym etapie rozwoju rynkowi bardziej opłacało się działać w modelu prostszym: sprowadzać gotowy materiał od zagranicznych podmiotów, przeprowadzać niezbędne działania po stronie wytwórczej (produktu leczniczego) i budować biznes wokół rejestracji oraz dystrybucji surowca farmaceutycznego. Wchodzenie w etap głębszego przetwórstwa (czyli zaczynając od API) w Polsce oznaczało większe ryzyko, większy koszt i dłuższy czas bez gwarancji zwrotu.
W dodatku na rynku konopi granice pojęciowe przez długi czas nie były dla wszystkich jasne. Gdzie kończy się materiał roślinny? W którym momencie zaczyna się substancja czynna? Co jeszcze jest etapem uprawy i pierwotnego przetwarzania, a co już etapem GMP? Dla podmiotu inwestującego miliony to są pytania fundamentalne, bo od odpowiedzi na nie zależy cały model obiektu, dokumentacji, odpowiedzialności i kosztów. Dojście do wypracowania stosownego modelu zabrało Instytutom wraz z przedsiębiorcami spory kawałek czasu.
3. Infrastruktura dla uprawy to nie jest kilka lamp i osuszacz
Jednym z najczęstszych uproszczeń, jakie widzę w rozmowach o krajowej uprawie, jest myślenie, że chodzi po prostu o wynajęcie hali, wstawienie regałów, lamp, kilku osuszaczy i zatrudnienie kilku osób. To nie ma nic wspólnego z rzeczywistością. Przez kilka lat zbierania doświadczenia w tej branży słyszeliśmy już naprawdę ciekawe propozycje i stwierdzenia takie jak „małe GMP”, „posadźmy to na polu a potem przetworzymy i oczyścimy”, „o klimat zadbamy osuszaczami powietrza”.
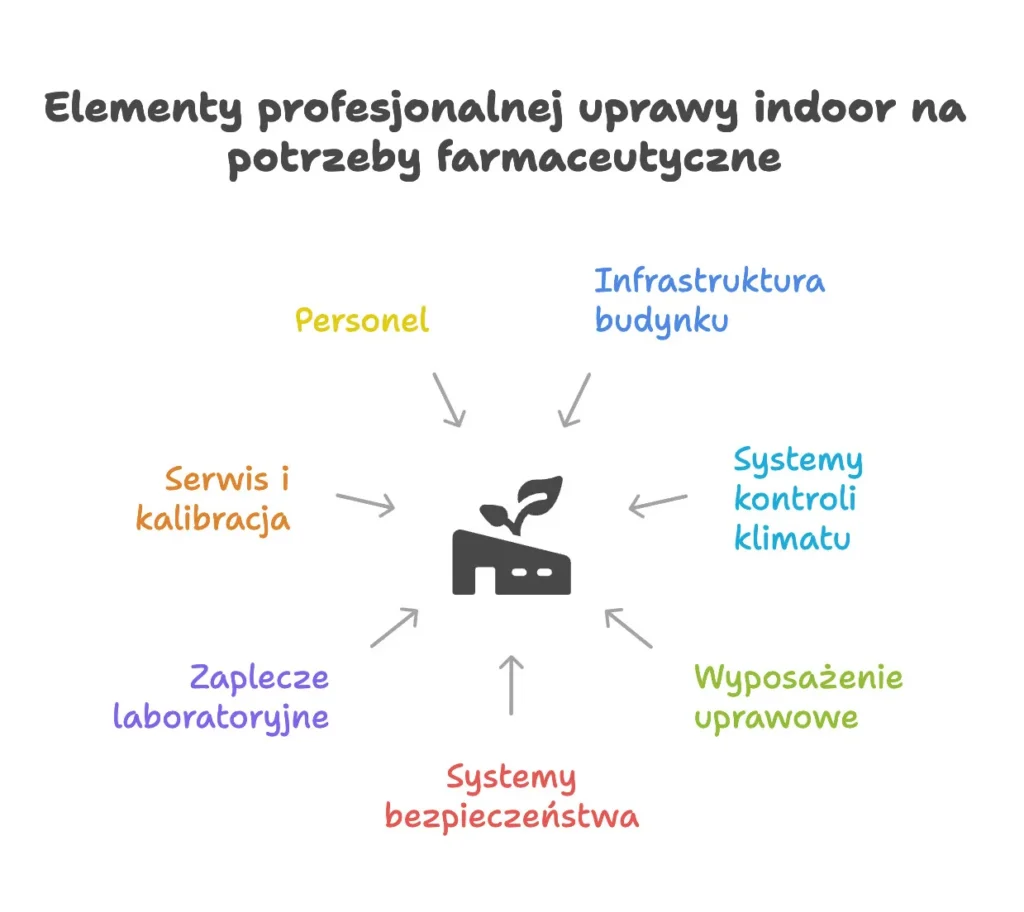
Profesjonalna uprawa indoor na potrzeby farmaceutyczne to infrastruktura kosztująca miliony złotych. I nie chodzi tylko o sam budynek. Chodzi o budynek odpowiednio wykończony, z materiałami odpornymi na wymagający mikroklimat, z powierzchniami nadającymi się do skutecznego mycia i dezynfekcji, z właściwym obiegiem ludzi i materiałów, z prawidłowo zaprojektowanym HVAC, filtracją powietrza, kontrolą temperatury, wilgotności, CO2, oświetlenia, nawodnienia, fertygacji i bezpieczeństwa.
Do tego dochodzi wyposażenie: regały uprawowe, lampy uprawowe, systemy sterowania klimatem, monitoring, zabezpieczenia, kontrola dostępu, systemy alarmowe, obszary suszenia, magazynowania i pakowania. Do tego laboratorium lub przynajmniej realny dostęp do kompetentnego zaplecza analitycznego. Później dochodzi do tego serwis, kalibracje, kwalifikacje instalacji i urządzeń. No i personel, osoby, które wiedzą, jak z tego korzystać. Z tego, czyli skomplikowanych systemów zarządzania fertygacją, HVAC, kontrolą dostępu i innymi peryferyjnymi systemami zarządzania budynkiem.
I właśnie tu wchodzi kolejna praktyczna bariera: nawet jeśli ktoś zbuduje obiekt, to jeszcze nie znaczy, że będzie umiał w nim pracować. Wdrożenie procedur nie polega na tym, że drukuje się SOP-y, podpisuje listę obecności ze szkolenia i uznaje temat za zamknięty. Personel musi te procedury przećwiczyć. Musi popełnić kontrolowane błędy na materiale testowym. Musi nauczyć się pracy w reżimie, w którym każda pomyłka ma znaczenie. Bez tego procedury będą wykonywane źle, mechanicznie albo pozornie. A przy roślinie i przy systemie jakości pozorność wychodzi bardzo szybko. W takim wypadku można albo zatrudnić konsultantów z zachodu, gdzie stawki sięgają 400 euro na godzinę, albo uczyć się na błędach.
Dlatego mówiąc uczciwie: sama infrastruktura GACP plus zdolność do sensownej pracy w takim systemie to koszt co najmniej kilku milionów złotych, zanim w ogóle zaczniemy mówić o stabilnej, powtarzalnej produkcji.
4. Uprawa i stabilność zaczynają się od biologii, ale kończą na powtarzalności
Uprawa konopi na potrzeby farmaceutyczne nie jest zwykłą ogrodniczą produkcją. To proces biologiczny poddany presji farmaceutycznej powtarzalności.
Najpierw trzeba wybrać model rozmnażania. Można iść w nasiona, można iść w klony z roślin matecznych, można pracować na materiale tkankowym, na przykład z agaru. Każda z tych metod ma swoje zalety i wady. Jedna daje większą jednorodność, ale wymaga innego nadzoru. Inna daje większą elastyczność, ale niesie ryzyko większego rozrzutu stabilności. Już na tym etapie trzeba wiedzieć, jaki cel jakościowy chce się osiągnąć.
Potem zaczyna się właściwa uprawa. I tu pojawia się kolejny problem praktyczny: rośliny trzeba prowadzić tak, żeby nie tylko urosły, ale żeby rosły w sposób porównywalny. Nie chodzi wyłącznie o plon. Chodzi o to, żeby końcowo uzyskiwać zbliżony profil kannabinoidowy, podobną jakość i podobne zachowanie materiału po zbiorze. To oznacza, że roślina musi być traktowana w możliwie taki sam sposób: to samo światło, ta sama temperatura, ta sama wilgotność, to samo nawożenie, to samo podłoże, ten sam trening, ta sama jakość wody, podobne warunki przepływu powietrza. Trzeba to pomnożyć przez liczbę roślin, liczbę pomieszczeń i liczbę cykli.
W teorii brzmi to banalnie. W rzeczywistości to jest przepis na bardzo trudne zadanie. Nawet w indoor rośliny nie zachowują się idealnie identycznie. Wpływ ma genetyka, presja biologiczna, mikroróżnice środowiskowe, błędy personelu, zmiana partii nawozów, problem z instalacją, a czasem zwykła ludzka nieuwaga. Sztuką nie jest wyhodować ładny kwiat. Sztuką jest zrobić to tak, żeby seria po serii mieścić się w oczekiwanej specyfikacji jakościowej.
A potem dochodzi jeszcze stabilność materiału. Susz konopny nie jest materiałem obojętnym. Reaguje na temperaturę, wilgoć, światło, tlen, sposób suszenia, czas przebywania w danym środowisku i sposób zapakowania i zawsze znajduje się na nim mikrobiologia (produkt nie jest i nigdy nie będzie sterlny). Z perspektywy jakości materiał zaczyna się starzeć wtedy, kiedy został doprowadzony do stanu docelowego, a nie wtedy, kiedy administracyjnie wygodnie nam zacząć o nim mówić jako „produkt końcowy”. Im dłużej trwa etap pośredni (wytwarzanie API), tym większe ryzyko, że stabilność i wyniki jakościowe zaczną pracować przeciwko nam.
5. Najważniejsza luka: brak krajowego etapu wytwarzania substancji czynnej
Do tej pory polski rynek rozwijał się głównie w modelu mniej ryzykownym. Podmiot kupował materiał z zagranicy, prowadził działania w ramach swojego modelu wytwórczego, wykonywał badania, przygotowywał dokumentację, przygotowywał i skłądał rejestrację i wprowadzał do obrotu surowiec farmaceutyczny. Ten model, mimo że formalnie wymagający, był biznesowo zrozumiały. Dlatego dało się go uruchamiać.
Nie wykształcił się natomiast krajowy etap, w którym ktoś bierze na siebie rolę rzeczywistego wytwórcy substancji czynnej dla konopi innych niż włókniste w oparciu o krajowy materiał z uprawy. A właśnie tu znajduje się największa luka systemu.
W praktyce taki etap oznacza przejęcie materiału po zbiorze i po wstępnym przygotowaniu, następnie wykonanie operacji takich jak trymowanie, dosuszanie do docelowych parametrów, standaryzacja procesu, kontrola jakości, odpowiednie pakowanie i przygotowanie materiału, który może wejść do dalszego legalnego łańcucha wytwórczego (czyli produkcji surowca farmaceutycznego).
I tu pojawia się elementarny problem i odpowiedź na pytanie dlaczego nie mamy jeszcze krajowego wytwórcy API. Gdy materiał jest importowany, trzeba uzyskać zgodę na jego przywóz, a następnie przejąć na siebie pełne ryzyko przetwarzania. Materiał startowy do procesu GACP nie jest jeszcze wysuszony do 10-12% zawartości wody, w związku z tym może się w trakcie transportu rozwijać mikrobiolgia. Jeżeli w trakcie etapu zamówiania i przetwarzania API coś pójdzie źle, straty są realne: czas, koszt, materiał, skrócenie daty ważności produktu, ryzyko odrzutu jakościowego. A oszczędność biznesowa na marży tego etapu często nie rekompensuje skali ryzyka. Mówiąc wprost: przez długi czas ten model po prostu się nie spinał.
Inaczej wyglądałaby sytuacja, gdyby działała produkcja krajowa. Wtedy materiał można byłoby przekazać do przetwarzania od razu, bez procedur importowych, bez oczekiwania i bez dodatkowych warstw ryzyka logistyczno-administracyjnego. Ale właśnie tego elementu dziś w Polsce brakuje.
6. Dostawcy, kwalifikacje i dokumenty, bez których nic nie istnieje
W GMP istnieje zasada, którą bardzo lubię przypominać: jeżeli czegoś nie zapisano, to to nie istnieje. W przypadku konopi ma to szczególne znaczenie, bo pracujemy nie tylko z produktem farmaceutycznym, ale też ze środkiem odurzającym, czyli z materiałem objętym dodatkowymi reżimami nadzoru i bezpieczeństwa.
To oznacza, że cały łańcuch dostaw musi być bezpieczny, przejrzysty i udokumentowany. Zaczyna się to już od materiału rozmnożeniowego. Kto dostarczył nasiona albo klony? W jaki sposób zostały zidentyfikowane? Jak potwierdzono ich jakość, pochodzenie i zgodność? Potem dochodzą kolejne elementy: kostki uprawowe, nawozy, woda, usługi DDD, transport, analityka laboratoryjna, serwis instalacji, kalibracje, odzież ochronna, opakowania i systemy zamknięcia.
Każdy z tych elementów wymaga kwalifikacji dostawcy albo przynajmniej odpowiedniego potwierdzenia, że jest pod kontrolą. W praktyce oznacza to setki dokumentów, oceny, umowy jakościowe, uzgodnienia techniczne, specyfikacje i raporty. A później trzeba to jeszcze utrzymać w ruchu, aktualizować i powiązać z odpowiedzialnością stron.
W modelu instytutowym pojawia się dodatkowa komplikacja: odpowiedzialność trzeba rozdzielić między instytut a wytwórcę GMP. Kto odpowiada za obiekt? Kto za personel? Kto za dokumentację? Kto za laboratorium? Kto za przekazanie materiału dalej? Kto za zabezpieczenia? Kto za audyt dostawców? Kto za jakość na danym etapie? To są rzeczy, które w klasycznej spółce można ułożyć wewnętrznie. Tutaj trzeba je jeszcze poukładać między podmiotami.
Im bardziej złożony jest łańcuch, tym wolniej wszystko idzie. A jeżeli dodatkowo pracujemy na środkach odurzających, dochodzi kolejna warstwa formalna, która skutecznie zabija iluzję, że da się to zrobić szybko.
7. Stabilność i rejestracja to nie formalność, tylko długi finał
Załóżmy nawet najbardziej optymistyczny scenariusz. Uprawa się udała (najczęściej 3krotnie w klasycznej kampani walidacyjnej procesu). Genetyka zachowuje się dobrze. Serie są stabilne, porównywalne, mieszczą się w zakładanych parametrach. Nie ma problemów mikrobiologicznych, nie ma katastrof procesowych, nie ma odchyleń, które wywracają projekt. To nadal nie oznacza, że produkt za chwilę wejdzie na rynek.
Najpierw trzeba wykonać serie rozruchowe, a następnie serie, które rzeczywiście posłużą do badań stabilności i walidacji procesu. Z punktu widzenia jakości i klasycznych standardów stabilności mówimy o badaniach opartych o co najmniej kilka partii oraz o horyzoncie dłuższym 3 miesiące.
Dodatkowo właśnie tutaj wychodzą wszystkie błędy wcześniejszych etapów. Materiał może źle znosić starzenie. Może okazać się zbyt wrażliwy na wilgoć. Może wykazywać niestabilność profilu. Mogą pojawić się problemy mikrobiologiczne charakterystyczne dla danego obiektu albo regionu. Mogą wyjść nieprzewidziane interakcje z opakowaniem lub systemem przechowywania. W branży konopi i w związku z tym, że pracujemy z rośliną o przeznaczeniu do inhalacji, naprawdę bardzo dużo rzeczy może pójść nieidealnie.
Dopiero gdy te etapy zostaną zakończone sensownie, można mówić o bezpiecznym wejściu w procedurę rejestracyjną do URPL. A sama procedura rejestracyjna też nie jest chwilą. Trwa, może być zatrzymywana pytaniami, może wymagać uzupełnień, może wymusić korektę dokumentacji, specyfikacji, opakowania, deklarowanego okresu ważności albo nawet opisu procesu. Innymi słowy: nawet przy idealnym przebiegu droga od przepisu do rynku jest długa. Przy realnym przebiegu jest jeszcze dłuższa. Sama procedura w URPL może trwać do 210 dni, przy założeniu że dokumentacja jest kompletna i nie jest wstrzymywany bieg rejestracji w celu uzpełnienia dokumentacji.
Wniosek
Dlaczego więc dziś nadal nie ma na rynku medycznych konopi wyprodukowanych w Polsce? Bo w Polsce otwarto możliwość uprawy, ale nie zbudowano jeszcze działającego, opłacalnego i jakościowo domkniętego modelu od rośliny do zarejestrowanego surowca farmaceutycznego.
Instytuty dostały uprawnienie, ale nie dostały prostego modelu inwestycyjnego. Rynek dostał legalność pierwszego etapu, ale nie dostał naturalnie działającego pomostu do etapu substancji czynnej i dalszego wytwarzania. Do tego doszły ogromne koszty infrastruktury, trudność w budowi zespołów, konieczność wdrożenia jakości na poziomie dużo wyższym niż klasyczna uprawa, ryzyko stabilności, złożoność dokumentacji i niska opłacalność wejścia w najbardziej ryzykowny etap procesu.
Mówiąc najprościej: ustawa otworzyła drzwi, ale za tymi drzwiami nadal trzeba zbudować cały zakład, system jakości, zespół, łańcuch dostaw i model biznesowy, który się obroni. I właśnie dlatego na dziś Polska nadal bardziej mówi o krajowej medycznej marihuanie, niż ją realnie wytwarza.

