Dobra Praktyka Laboratoryjna (GLP) to międzynarodowy system zapewnienia jakości w badaniach nieklinicznych, który nakłada surowe reguły dotyczące planowania, prowadzenia i dokumentowania eksperymentów. Dokumentacja GLP jest kręgosłupem tego systemu – musi odzwierciedlać wszystkie procedury, instrukcje oraz zapisy wyników i decyzji. Dzięki przejrzystej dokumentacji systemu jakości GLP zapewniasz powtarzalność badań, rzetelność danych oraz zgodność z przepisami. GLP obejmuje m.in. badania toksykologiczne substancji chemicznych, leków, kosmetyków i środków ochrony roślin, aby zapewnić ochronę zdrowia ludzi i środowiska. Większość laboratoriów aspiruje do wpisania na listę certyfikowanych jednostek GLP, co wiąże się z dodatkowymi wymaganiami formalnymi. Prawidłowa dokumentacja GLP nie jest więc tylko formalnością, ale i dowodem profesjonalizmu i wiarygodności wyników, który ułatwia także współpracę z partnerami i klientami z całego świata.
Tworząc dokumentację GLP, nie warto traktować tego jako jednorazowego obowiązku na czas inspekcji. Lepiej przyjąć podejście ciągłego doskonalenia: regularnie aktualizować procedury, szkolić personel i reagować na uwagi auditorów. Większość laboratoriów GLP korzysta również z gotowych szablonów dokumentów lub dedykowanych systemów QMS i LIMS, które wspierają organizację dokumentacji. Można też zlecić konsultacje zewnętrznym ekspertom, aby zweryfikować, że przygotowana dokumentacja spełnia wszystkie wymogi. Taka kultura jakości sprawia, że dokumentacja jest zawsze kompletna i wiarygodna, a laboratorium pewne swojej zgodności. W kolejnych rozdziałach opisujemy szczegółowo, co powinna zawierać dokumentacja GLP, jak ją przygotować krok po kroku oraz na co zwrócić uwagę, aby uniknąć typowych błędów.
Kluczowe elementy dokumentacji GLP
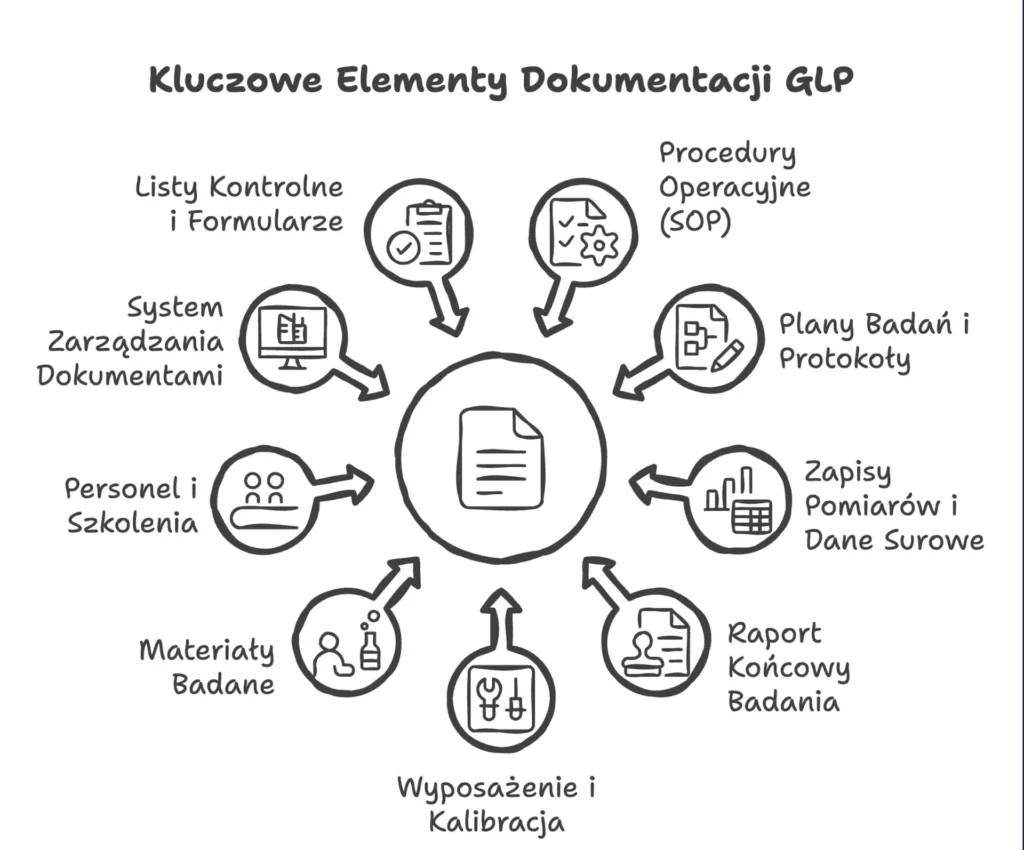
Dokumentacja systemu jakości GLP obejmuje wszystkie fazy i obszary badań – od przyjęcia próbki po archiwizację danych. Każdy etap procesu badawczego musi być odpowiednio udokumentowany i zgodny z obowiązującymi procedurami. Krytyczne elementy takiej dokumentacji to m.in.:
- Procedury operacyjne (SOP) – szczegółowe instrukcje opisujące wykonywanie każdej czynności laboratoryjnej (np. przyjmowanie i przygotowywanie próbek, obsługa urządzeń, metody analityczne, zasady bezpieczeństwa, zarządzanie dokumentacją). Dobrze napisane SOP gwarantują powtarzalność i standaryzację pracy oraz minimalizują ryzyko pomyłek. Na przykład SOP może określać dokładne parametry pomiaru, takie jak temperatura czy czas analizy, aby każdy analityk otrzymał porównywalne wyniki. Każda procedura GLP musi być formalnie zatwierdzona i mieć przypisane numery wersji.
- Plany badań i protokoły – dokumenty przygotowywane przed rozpoczęciem eksperymentów, określające cel, zakres, metodykę i harmonogram badania. Na podstawie planu badania laboranci wiedzą, jakie kroki wykonać, a kierownik badania może śledzić postęp. Protokoły muszą być zatwierdzone przez wszystkie odpowiednie osoby (kierownika badania, QA, klienta). W GLP zmiana planu po rozpoczęciu badania wymaga formalnego zatwierdzenia i udokumentowania (proces odstępstw).
- Zapisy pomiarów i dane surowe – wszystkie pozyskane wyniki i obserwacje, zapisywane na bieżąco w dziennikach laboratoryjnych, formularzach czy zwalidowanych systemach elektronicznych. Każdy wpis powinien zawierać datę i podpis osoby wykonującej pomiary. Konieczne jest także jednoznaczne oznaczenie próbek oraz ich numeracja. Dodatkowo, wszelkie surowe dane warto archiwizować w formie elektronicznej (backup), by zabezpieczyć je przed utratą. Warto również przechowywać kopie wyników w systemie LIMS lub skany papierowych zapisów, co zapewnia dodatkową warstwę bezpieczeństwa danych.
- Raport końcowy badania – kompleksowe sprawozdanie zestawiające przebieg eksperymentu, zastosowane metody, wyniki i wnioski końcowe. Raport końcowy stanowi oficjalne podsumowanie badania i musi być przygotowany zgodnie z wytycznymi GLP (struktura dokumentu, oświadczenie o zgodności). Każde sprawozdanie powinno zawierać oświadczenie kierownika badania potwierdzające przestrzeganie wszystkich procedur oraz zostać podpisane i zatwierdzone przez kierownika badania oraz zaopiniowane pozytywnie przez jednostkę zapewnienia jakości (QA).
- Wyposażenie i kalibracja – rejestr używanych urządzeń i aparatury wraz z zapisami przeglądów technicznych, konserwacji, napraw oraz kalibracji. Dokumentacja ta dowodzi, że sprzęt był odpowiedni do wykonania badań. Należy archiwizować certyfikaty kalibracji, instrukcje obsługi oraz harmonogramy serwisowe. Niedokładna ewidencja sprzętu lub zaniedbania przy kalibracji mogą spowodować nieważność uzyskanych wyników. Harmonogramy kalibracji należy uaktualniać i dokumentować, a kopie certyfikatów przechowywać w rejestrze. Wagi muszą być przesyłane z odpowiednią częstotliwością do legalizacji. Wykonywanie badań na źle skalibrowanym sprzęcie lub nieskalibrowanym sprzęcie może wpłynąć na podważenie wyników badań przez podmioty sprawdzające.
- Materiały badane, odniesienia i odczynniki – ewidencja przyjmowanych substancji, materiałów odniesienia i odczynników. Każdy materiał musi być oznakowany (nr partii, data ważności) i opisany (pochodzenie, stężenie, czystość). Laboratorium powinno prowadzić bilans ilości przyjętych i zużytych materiałów, aby mieć pełną kontrolę nad stanem zapasów. Wykaz odczynników i ich paragonów czy faktur również powinien być przechowywany. Co więcej, GLP wymaga, aby warunki przechowywania materiałów (np. temperatura, wilgotność) były odpowiednio dokumentowane, co gwarantuje stabilność próbek.
- Personel i szkolenia – rejestr zatrudnionych osób z informacjami o kwalifikacjach, doświadczeniu i ukończonych szkoleniach. GLP wymaga, by każdy pracownik był przeszkolony z zakresu swoich zadań oraz zasad GLP. Należy prowadzić zapisy obecności na szkoleniach, testów wiedzy, a także śledzić matrycę kompetencji (przyporządkowanie zadań do osób). Dokumenty te zapewniają audytorom, że zespół ma wymagane kompetencje. Dodatkowo, każda zmiana personelu w trakcie badania powinna być odnotowana, a osoby zastępujące muszą spełniać te same wymagania kompetencyjne.
- System zarządzania dokumentami – procedury kontrolujące obieg dokumentów: numerację, wersjonowanie, zatwierdzanie, dystrybucję oraz archiwizację. Taki system zapobiega korzystaniu z nieaktualnych instrukcji. Ważne jest, aby wszystkie dokumenty posiadały wyraźnie oznaczone wersje i daty. Zwykle stosuje się elektroniczne narzędzia do zarządzania dokumentacją, które automatycznie śledzą zmiany i powiadamiają użytkowników o nowych wersjach. Przykładowo, system taki może wysyłać przypomnienia o terminie przeglądu procedury lub wymagać elektronicznego podpisu zatwierdzającego nową wersję.
- Listy kontrolne i formularze procesu – dodatkowe arkusze i listy kontrolne pomagają potwierdzić wykonanie wszystkich wymaganych kroków badania. Dzięki nim audytorzy widzą, że żaden etap nie został pominięty i mogą łatwo śledzić zgodność z planem badania.
Komputeryzacja i zabezpieczenia: Coraz więcej laboratoriów prowadzi część dokumentacji w formie elektronicznej. Wszystkie skomputeryzowane systemy (bazy danych, oprogramowanie analityczne, LIMS) muszą być zweryfikowane i odpowiednio zabezpieczone. Należy zapewnić integralność danych elektronicznych poprzez kontrolę dostępu, zapisy logów oraz wykonywanie backupów. W praktyce GLP akceptuje dokumentację elektroniczną (np. skany zapisów, podpisy cyfrowe) pod warunkiem spełnienia dodatkowych norm (np. 21 CFR Part 11). Dobrze wdrożony system pozwala zastąpić część papierologii i przyspiesza dostęp do danych. GLP wymaga jednak, aby każdy elektroniczny system był odpowiednio zwalidowany przed zastosowaniem. Przykładowo można stosować systemy LIMS wyposażone w automatyczne zapisy (audit trail), aby zapewnić pełną transparentność zmian.
Archiwizacja dokumentacji GLP
Dopełnieniem dokumentacji jest prawidłowe przechowywanie materiałów po zakończeniu badań. Raporty końcowe, dane źródłowe, protokoły, karty techniczne oraz użyte materiały trzeba przechowywać przez określony czas (zwykle co najmniej 5 lat od zakończenia projektu, a czasem dłużej w zależności od przepisów czy umów z klientem). Archiwum powinno być zabezpieczone przed zniszczeniem i dostępne tylko dla upoważnionych osób (zamknięte szafy, sejfy, kontrola wejścia do pomieszczenia). Archiwum powinno być też przechowywane w odpowiednich warunkach środowiskowych (stabilna temperatura i wilgotność), aby zapobiec uszkodzeniu dokumentów. Niezbędne jest też odpowiednie oznakowanie i katalogowanie dokumentów, tak aby w razie potrzeby można było łatwo odtworzyć cały przebieg badania. Dodatkowo do archiwum przekazywane są także finalne próbki i materiały badane, które muszą być zabezpieczone w odpowiednich warunkach (np. odpowiednia temperatura). W praktyce pomieszczenia archiwum powinny być klimatyzowane i wyposażone w monitoring, aby zminimalizować ryzyko zniszczenia dokumentów i próbek. W większych laboratoriach często tworzy się specjalne komórki (archiwum GLP) odpowiedzialne za nadzór nad tym procesem.
Rola jednostki Zapewnienia Jakości (QA)
Niezależna jednostka Zapewnienia Jakości to obowiązkowy element systemu GLP. Pracownicy QA nie realizują badań, lecz monitorują zgodność wszystkich procesów z zasadami GLP. W praktyce oznacza to przegląd zatwierdzonych planów badań, kontrolę przestrzegania SOP oraz ocenę raportów końcowych. QA przeprowadza inspekcje wewnętrzne i audyty dokumentacji – sporządza raporty z tych kontroli, które zawierają ewentualne niezgodności i zalecane działania korygujące. QA weryfikuje, czy w planie badania zdefiniowano kryteria akceptacji wyników oraz czy wszelkie problemy zostały dokładnie opisane w dokumentach. Ponadto QA monitoruje terminy badań – jeśli projekt przekracza planowany czas, zwraca uwagę na obowiązki związane z przedłużeniem badania. Raporty wewnętrzne QA oraz protokoły audytów dołączane są do dokumentacji badania, potwierdzając, że laboratorium nieustannie sprawdza i podnosi jakość swoich procedur.
Jak przygotować dokumentację GLP krok po kroku
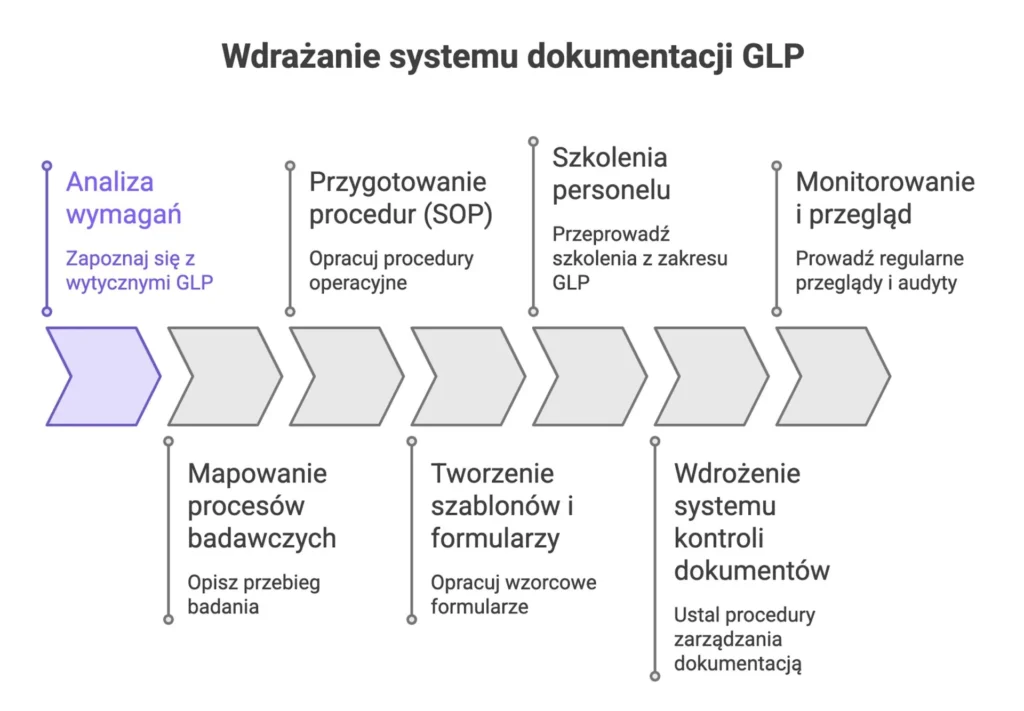
Utworzenie dokumentacji zgodnej z GLP wymaga uporządkowanego podejścia i współpracy całego zespołu. Zadania warto realizować etapami, aby stopniowo uwzględnić wszystkie niezbędne elementy. Poniżej prezentujemy przykładowe kroki przygotowania dokumentów:
- Analiza wymagań – Zapoznaj się dokładnie z wytycznymi GLP (np. rozporządzenie Ministra Zdrowia, wytyczne OECD) i określ zakres swojej dokumentacji. Ustal, jakie badania wykonujesz i jakie dokumenty będą potrzebne (np. listy kontrolne, procedury bezpieczeństwa, specyfikacje metod).
- Mapowanie procesów badawczych – Opisz w formie mapy lub schematu przebieg typowego badania w Twoim laboratorium: od przyjęcia i rejestracji próbki, przez przygotowanie i analizę, aż po raport końcowy i archiwizację. Wyznaczenie etapów umożliwi zidentyfikowanie momentów, gdzie potrzebne są szczegółowe SOP, formularze czy rejestry.
- Przygotowanie procedur (SOP) – Opracuj lub dostosuj procedury operacyjne dla każdej kluczowej czynności. Każdy SOP powinien zawierać cel, zakres, kryteria akceptacji oraz opis krok po kroku wykonywanych zadań. Pamiętaj, aby uwzględnić kwestie bezpieczeństwa i zgodność z przepisami. Po napisaniu, przeprowadź formalny proces zatwierdzania: dopisz nagłówki z numerem wersji, datą i podpisami osób odpowiedzialnych. Udostępnij zatwierdzone SOP pracownikom i przechowuj starsze wersje w archiwum.
- Tworzenie szablonów i formularzy – Opracuj wzorcowe formularze do gromadzenia danych: np. karty obserwacji, dzienniki pracy, karty kontrolne czy specyfikacje analityczne. Uporządkowane formaty (np. tabele z rubrykami na daty i podpisy) pomagają zespołowi prowadzić jednoznaczne zapisy. Dzięki użyciu standardowych szablonów łatwiej uniknąć błędów przy wypełnianiu danych i zapewnić, że żaden istotny parametr nie zostanie pominięty.
- Szkolenia personelu – Przeprowadź szkolenia z zakresu nowych procedur, formularzy i zasad GLP. W trakcie szkolenia wyjaśnij pracownikom oczekiwania dotyczące dokumentacji (np. konieczność podpisywania każdego wpisu czy stosowania właściwych kodów próbki). Po szkoleniu zbierz potwierdzenia (listy obecności, testy) potwierdzające uczestnictwo i zrozumienie materiału. Regularnie aktualizuj te zapisy szkoleń, aby każdy miał udokumentowane kwalifikacje adekwatne do swoich zadań.
- Wdrożenie systemu kontroli dokumentów – Ustal procedury zarządzania dokumentacją: kto zatwierdza nowe wersje, jak dokumenty są rozpowszechniane oraz jak przechowywane. Dobrą praktyką jest ustanowienie rejestru dokumentów z unikalnym numerem i wersją. Wprowadź praktykę, że każdy pracownik korzysta tylko z aktualnych wydruków lub wersji elektronicznych dokumentów. Jeśli to możliwe, warto skorzystać z narzędzi elektronicznych wspierających kontrolę obiegu dokumentów (np. systemów QMS).
- Monitorowanie i przegląd – Po uruchomieniu dokumentacji prowadź regularne przeglądy i audyty wewnętrzne. Sprawdzaj, czy procedury są stosowane w praktyce i czy dokumenty są prawidłowo wypełniane. Raportuj wszelkie niezgodności oraz podejmuj działania korygujące – modyfikuj procedury i szkolenia według potrzeb. Dzięki temu system dokumentacji będzie się usprawniał z każdym kolejnym cyklem badawczym.
Najczęstsze błędy w dokumentacji GLP
Przygotowując system dokumentacji, należy zadbać o jasność i kompletność. Jednym z najczęstszych błędów jest korzystanie z nieaktualnych wersji dokumentów lub brak ich wersjonowania. Ważne jest również formalne dokumentowanie wszelkich zmian i odchyleń. Oto przykłady pułapek do uniknięcia:
- Brak spójności dokumentacji – korzystanie z nieaktualnych formularzy lub SOP bez oznaczeń wersji prowadzi do sprzeczności i trudności podczas audytów. W GLP każda zmiana musi być śledzona i archiwizowana.
- Niedokładne zapisy – pomijanie podpisów, dat lub prowadzenie nieczytelnych notatek osłabia wiarygodność danych. Wszystkie wpisy (w dziennikach, formularzach) muszą być kompletne, czytelne i opatrzone datą oraz podpisem. Błędy w zapisie mogą skutkować koniecznością odwołania wyników pomiaru.
- Nieformalna komunikacja zmian – ważne ustalenia robocze zapisane jedynie ustnie lub na tymczasowych notatkach nie spełniają wymogów GLP. Zmiany w procedurach powinny przechodzić formalną ścieżkę zatwierdzania (np. aneks do SOP podpisany przez odpowiednie osoby).
- Brak archiwizacji wcześniejszych wersji – konieczne jest zachowanie starszych wersji SOP, protokołów i raportów. Niewłaściwe przechowywanie lub brak dostępu do archiwum uniemożliwia odtworzenie przeszłych procesów badawczych i podważa wiarygodność badań.
- Niedokumentowanie odstępstw – każdy przypadek odchylenia od planu badania lub procedury musi być opisany, przeanalizowany i zatwierdzony. Ignorowanie lub niedokładne opisanie problemów (odstępstw) podważa integralność wyników badania i jest poważnym uchybieniem w GLP. Odchylenia powinny być opisane w raporcie odstępstw, zatwierdzone przez kierownika oraz ocenione przez QA pod kątem wpływu na wyniki.
- Brak jasnych odpowiedzialności – nieprzypisanie konkretnych osób do nadzoru nad dokumentacją (np. archiwum, QA) prowadzi do zaniedbań. W GLP każda czynność dokumentacyjna powinna mieć wyraźnie określonego opiekuna (kierownik badania, inspektor QA itp.).
- Niewłaściwe poprawki w zapisach – przekreślanie lub zamazywanie danych bez podania daty i podpisu osoby poprawiającej jest niedopuszczalne. W GLP każda korekta powinna być wprowadzona przejrzyście: oryginalny wpis musi pozostać czytelny, a obok wpisuje się poprawioną wartość wraz z datą i podpisem osoby nanoszącej zmianę.
- Brak zabezpieczeń dokumentacji – brak kontroli dostępu do archiwum lub systemów elektronicznych (np. brak haseł, zamków) może prowadzić do utraty lub nieautoryzowanej modyfikacji danych. Dokumenty GLP należy przechowywać w zabezpieczonych miejscach, a dostęp do nich ograniczać tylko do uprawnionych osób.
- Brak formalnego wsparcia kierownictwa – system jakości GLP powinien być zatwierdzony przez najwyższe kierownictwo laboratorium (np. w formie polityki jakości lub zarządzenia). Brak takiego formalnego zatwierdzenia osłabia autorytet procedur i może prowadzić do problemów w ich egzekwowaniu.
Przygotowanie dokumentacyjne do inspekcji GLP
Inspekcja GLP to formalne sprawdzenie zgodności laboratorium z obowiązującymi przepisami. Warto przygotować się zawczasu: przeprowadzić wewnętrzny audyt, uporządkować dokumenty i upewnić się, że wszystkie kluczowe zapisy są kompletne. Inspektorzy często wymagają wglądu w następujące dokumenty i rejestry:
- Aktualne wersje SOP i planów badań – wraz z dowodami zatwierdzeń (podpisy, daty) oraz ewentualnymi aneksami i raportami odstępstw.
- Dzienniki laboratoryjne i dane surowe – oryginały zapisków wraz z podpisami i datami. Przedstaw pełen łańcuch danych pomiarowych, w tym wykresy, zrzuty ekranów czy zapisy z urządzeń pomiarowych. Każdy wpis powinien odnosić się do konkretnego punktu planu badania.
- Raporty końcowe badania – kompletne sprawozdania z analiz, podpisane przez kierownika badania i odzwierciedlające wszelkie problemy napotkane podczas badania. Upewnij się, że wszystkie sekcje raportu (metody, wyniki, omówienie) są wypełnione.
- Rejestr urządzeń i certyfikaty kalibracji – dowody wykonania kalibracji/serwisu sprzętu używanego w badaniu, co potwierdzi poprawność pomiarów.
- Zapisy szkoleń i kwalifikacji personelu – listy obecności na szkoleniach oraz świadectwa i certyfikaty. Dla każdej osoby inspektorzy oczekują dokumentacji potwierdzającej znajomość procedur.
- Protokoły QA i dokumenty wewnętrznych audytów – raporty z inspekcji wewnętrznych i wyniki oceny systemu, które potwierdzają działania zapewnienia jakości.
Utrzymywanie kompletnej dokumentacji przez cały czas umożliwia płynną współpracę z organami nadzoru. Dzięki temu możesz szybko udostępnić potrzebne informacje i uniknąć opóźnień w procesie weryfikacji.
Korzyści z dobrej dokumentacji GLP
Dokładna i zgodna dokumentacja GLP to oprócz wymogu prawnego sprawne narzędzie biznesowe. Przejrzysta dokumentacja pozwala zoptymalizować procesy badawcze i skrócić czas potrzebny na przygotowanie wyników. Firmy, które dbają o wiarygodne dane, budują większe zaufanie klientów i regulatorów, co sprzyja szybkiemu wprowadzaniu nowych produktów na rynek. Dobre praktyki dokumentacyjne zwiększają efektywność pracy w laboratorium – gdy każdy wie, gdzie szukać informacji, dzięki czemu unikasz powtarzalnych błędów i szybciej reagujesz na nowe wymagania. Ponadto spójne procedury ułatwiają identyfikację obszarów do poprawy i optymalizację kolejnych procesów.
Podsumowanie
Sporządzenie i utrzymanie dokumentacji systemu jakości zgodnej z GLP to proces wymagający konsekwencji i dbałości o szczegóły. Dobrze opracowane procedury, protokoły i raporty pozwalają zachować zgodność z regulacjami oraz usprawniają codzienną pracę w laboratorium.
Oferujemy kompleksowe wsparcie i szkolenia, dzięki którym Twoja dokumentacja GLP będzie zawsze aktualna i gotowa na każdą kontrolę. Zapraszamy do kontaktu – nasi eksperci odpowiedzą na wszystkie pytania i pomogą wdrożyć system GLP w Twoim laboratorium.

