W ADVISK lubimy się kierować prostymi zasadami: jeśli regulator coś pisze publicznie, to nie dlatego, że ma wolny wieczór i chce się podzielić prozą życia. Warning letter to klarowny sygnał alarmujący – realne ryzyko dla pacjenta, jakości albo integralności systemu. Dlatego te listy są tak cenne dla całej branży. Oczywiście nigdy, przenigdy nie chcesz zobaczyć nazwy swojej firmy w nagłówku takiego pisma, dlatego wychodzimy z założenia, że zawsze warto je analizować i wyciągać z nich wnioski.
Ten artykuł przygotowaliśmy dla publiczności z branży life science: QA/QC, produkcji, inżynierii, CSV/IT, RA, a także osób zarządzających. Pisząc ten artykuł trzymamy się perspektywy naszego doświadczenia. Nie będziemy udawać, że “wdrożenie CAPA” to trzy kliknięcia w systemie i magiczny podpis. Z doświadczenia doradczego wiemy, że tam, gdzie w papierach “jest super”, w rzeczywistości często jest: dobra, działamy, tylko nie teraz, bo mamy kampanię / walidację / brak ludzi / właśnie padł autoklaw. Podsumujemy czego regulator szuka w 2026 roku, jakie wzorce przewijają się FDA po wdrożeniu systemu AI nadzorującego bazę podmiotów wytwarzających leki.
Uwaga: jesteśmy w marcu, więc 2026 to na razie “początek sezonu”. Ale nawet na początku sezonu widać, gdzie FDA potrafi podkręcić tempo.
Co czytamy warning letters w 2026
Na początku 2026 w listach ostrzegawczych wydanych do firm farmaceutycznych wyraźnie widać, że regulator patrzy już mniej na pojedyncze “wpadki”, a bardziej na stan kontroli procesu i dojrzałość systemu jakości. To jest ważna zmiana mentalna. Jeśli masz odchylenie, ale umiesz je złapać, przeanalizować, wytłuścić ryzyko, wdrożyć działania i realnie sprawdzić skuteczność = to zwykle da się obronić tezę, że organizacja jest “pod kontrolą”. Jeśli natomiast dowody są poszarpane, trendów nikt nie łączy kropkami w przeglądach produktu czy przeglądach systemu jakości, a CAPA jest bardziej deklaracją niż mechanizmem – wtedy pada znane pytanie „pokażcie mi najdłużej otwarte CAPA/odchylenie w ostatnich X miesięcy”.. a wtedy robi się gorąco w war roomie inspekcyjnym.
Zauważamy w tym roku kilka mocnych sygnałów:
Po pierwsze: sterylność i aseptyka nadal są “na radarze” nie tylko w klasycznych wytwórniach, ale też (a może nawet szczególnie) u podmiotów kontraktowych i w obszarach, które czasem same o sobie mówią “my tylko robimy X, to nie jest pełna produkcja”. W listach przewijają się tematy takie jak kontrola aseptyczna w RABS/ISO 5, utrzymanie bariery, zachowanie first air, smoke studies, media fills, monitoring środowiska i sensowna reakcja na trendy mikrobiologiczne.
Po drugie: media, a szczególnie woda i powiązane instalacje, są traktowane tak, jak powinny: jak surowiec krytyczny, a nie “tło techniczne”. Warto wrócić do analizy ryzyka dla krytycznych mediów. Nie “woda z pętli”, tylko “komponent procesu o wymaganiach jakościowych”. Sama zmiana słów potrafi zmienić decyzje inwestycyjne.
Po trzecie: laboratorium i data integrity. I tu FDA jest naprawdę bezlitosne: brak surowych danych, brak pełnej ścieżki, notatki “poza systemem”, backdating, zmiany wyników bez śladu, niszczenie papierów, utrudnianie inspekcji – to są czerwone flagi, które potrafią przykryć nawet niezłe wyniki jakościowe. Bo bez wiarygodnych danych nie ma wiarygodnej jakości.
Po czwarte: dochodzenia, OOS, reklamacje i CAPA. W 2026 nadal widać, że wiele organizacji jest świetnych w odpieraniu piłki słowami (“nie stwierdzono wpływu”), ale dużo słabszych w naukowym udowodnieniu, że wpływu faktycznie nie ma. A regulator (bez znaczenia czy FDA, czy GIF) bardzo lubi pytania typu: “skąd wiesz?” i “pokaż dowód”.
Po piąte: zwolnienie serii i specyfikacje. Brzmi jak fundament i… dokładnie tak nim jest. W listach przewijają się sytuacje, gdzie brakuje badań kluczowych atrybutów jakości (tożsamość, moc, zanieczyszczenia, mikrobiologia), albo kryteria zwolnienia są niepełne. I to nie jest problem “laboratorium”, tylko błędnie wykonanej analizy ryzyka dla procesu i produktu.
Jeśli w 2026 ktoś nadal łudzi się, że “jakoś to będzie” jest strategią jakości, to mamy złą wiadomość – FDA nie przyjmuje “jakoś” jako jednostki miary.
Playbook ADVISK: jak przełożyć trendy na konkretne działania
Poniżej proponujemy plan działań, który stosujemy jako logikę projektową w firmach przygotowujących się do audytów, inspekcji lub dużych programów usprawnień. To nie jest “jedyny słuszny” plan, ale jest pragmatyczny i odporny na realia typu: “brak zasobów”, “pilne serie”, “system w trakcie walidacji”.
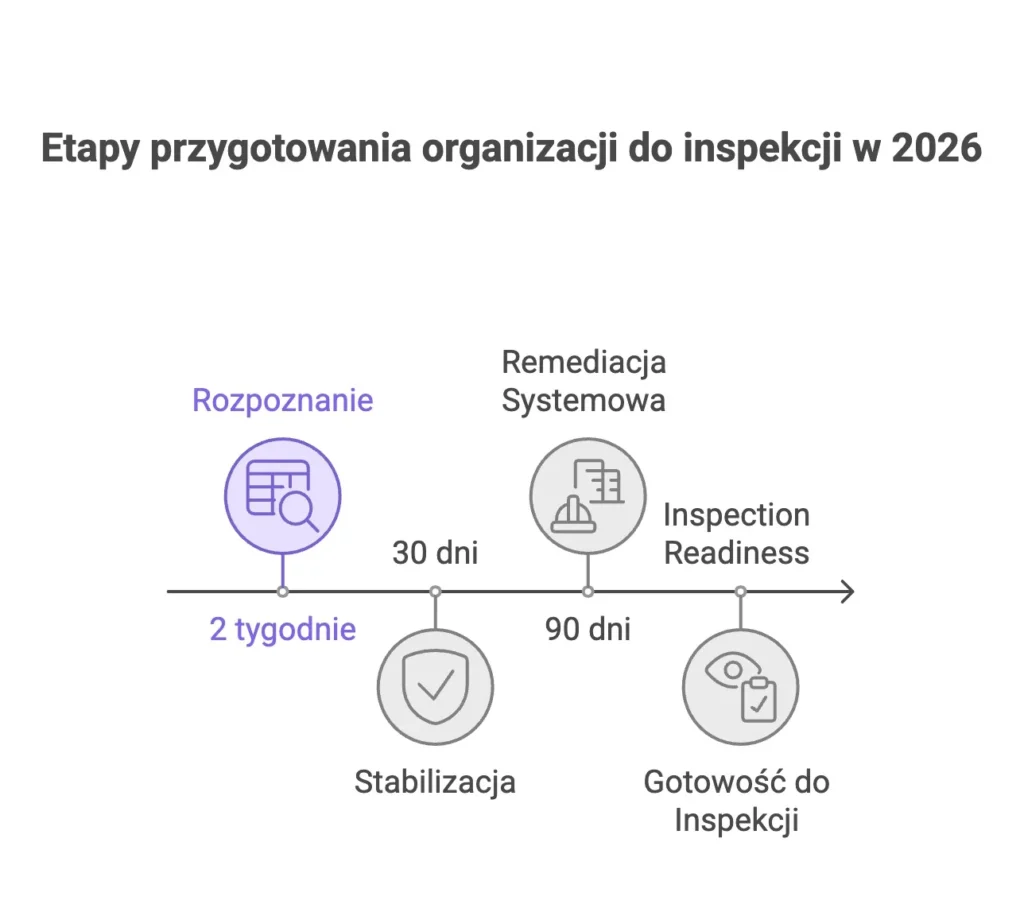
Etap rozpoznania: dwa tygodnie prawdy
Zaczynamy od przeglądu danych, bo dane nie kłamią (najwyżej ich nie ma). Najpierw identyfikujemy obszary, które najczęściej wywołują eskalacje: aseptyka/EM, woda i utilities, data integrity, OOS/odchylenia/reklamacje, zwolnienie serii, nadzór nad podwykonawcami. Następnie robimy szybkie “mapowanie dowodów”: jakie są trendy, gdzie są dziury, czy decyzje jakościowe mają uzasadnienie, czy CAPA ma weryfikację skuteczności, czy dział jakości ma realną władzę, czy tylko “odpowiedzialność w opisie stanowiska”.
W praktyce już na tym etapie wychodzą rzeczy bolesne, ale cenne: np. próbki środowiskowe zbierane i zapisywane zgodnie z procedurami, ale nie trendowane; OOS “zamykane” bez weryfikacji wpływu na inne serie; system wody kwalifikowany, ale wyniki “na czerwono” normalizowane komentarzem; audit trail niby jest, ale nikt go nie przegląda.
Etap stabilizacji: trzydzieści dni szybkich wygranych
Na tym etapie zabieramy się za tematy, które najszybciej obniżają ryzyko: porządkujemy retencję danych (papier i elektronika), przykładowo blokujemy praktyki “poza systemem” (zeszyty prywatne, pre-podpisy, backdating), ustawiamy minimalny standard reakcji na odchylenia monitoringu środowiskowego i niepokojące trendy, poprawiamy triage odchyleń i OOS, robimy ponowny przegląd i określamy podstawowe role i odpowiedzialności działu jakości.
Jeśli organizacja działa w warunkach sterlnych tu często wchodzi też “higiena aseptyczna”: interwencje, gowning, przepływy, smoke studies (jeśli nieaktualne lub niepewne), sensowne planowanie APS (media fills) i ocena “co jest krytyczne” vs “co jest formalnością”. W aseptyce formalność bywa iluzją, a mikrobiologia ma brutalnie pragmatyczne podejście do świata.
Etap remediacji: dziewięćdziesiąt dni pracy systemowej
Tu wchodzą tematy trudniejsze: ponowna kwalifikacja instalacji (woda, pętle, punkty użycia, eliminacja dead-legów), przebudowa programu monitoringowego (nie tylko “ile i gdzie próbkujemy”, ale też jak interpretujemy trendy i jak reagujemy, jak tworzymy kulodporną analizę ryzyka i wyłapujemy wszystkie ryzyka dla danej klasy czystości), wzmocnienie walidacji i kwalifikacji (w tym walidacja procesu i utrzymanie stanu kontroli), dopięcie nadzoru nad podwykonawcami (quality agreements “żywe”, a nie “do szuflady”).
W tym etapie często pojawia się też pytanie o narzędzia cyfrowe: czy potrzebujemy czegoś nowego, odświeżenia eQMS, LIMS, narzędzi do monitoringu środowiskowego, narzędzi do zarządzania zmianą i odchyleniami, narzędzi do zarządzania walidacją/CSV. Nasza perspektywa jest prosta: narzędzie ma wspierać proces i dowodowość, a nie maskować chaos. PS tak, da się te działania zrobić szybko, skutecznie i prawidłowo w 90 dni.
Etap “inspection readiness”: ćwiczenia z trudnych pytań
Na koniec robimy to, co często jest pomijane: trening inspekcyjny oparty o dowody. Nie “co powiemy”, tylko “co pokażemy”. Przechodzimy po krytycznych ścieżkach: odchylenie → dochodzenie → CAPA → weryfikacja skuteczności; trend monitoringu → decyzja jakościowa; odchylenie wyników dla wody → impact assessment; OOS → rozszerzenie zakresu; problem z dostawcą → eskalacja i decyzje. Dla wielu zespołów to jest moment otrzeźwienia – nagle widać, gdzie procedura jest piękna, ale brakuje jej dowodów.
Co to listy ostrzegawcze FDA oznaczają dla Polskich firm z przemysłu regulowanego
Polskie organizacje mają często miks realiów: działamy według EU GMP, mamy klientów globalnych, a do tego część zakładów realnie “pracuje na USA” (eksport, kontrakty, łańcuch dostaw, analityka). I teraz ważny punkt: nie chodzi o to, żeby robić dwa równoległe systemy jakości (“EU system” i “FDA system”). To jest droga do kosztów i sprzeczności. Chodzi o to, żeby zbudować jeden system, który jest wystarczająco dojrzały i dowodowy, żeby przejść zarówno wymagania EU, jak i oczekiwania FDA.
W praktyce 2026 to dobry moment, żeby spojrzeć na to przez pryzmat trzech wspólnych mianowników:
Contamination Control Strategy jako logika zarządzania sterylnością
W UE od nowelizacji aneksu 1 mamy mocny nacisk na CCS i podejście w stylu: ryzyko–kontrole–monitoring–przegląd. Nawet jeśli Twoja organizacja nie produkuje sterylnie, filozofia CCS przydaje się w wielu obszarach:,produkty biologiczne, środowiska krytyczne, procesy wrażliwe na zanieczyszczenia. Dla polskich firm to jest też praktyczny “język wspólny” z klientami zagranicznymi, którzy oczekują spójnego podejścia do ryzyka związanego z wytwarzaniem.
Quality Risk Management bez “uznaniowości”
Jeśli ryzyko jest oceniane raz tak, raz inaczej (bo różni ludzie, różne skale, różne nastroje), to w 2026 będzie coraz trudniej to obronić. Trendy regulatorów idą w stronę tego, żeby ograniczać subiektywność w QRM i mieć sensowną formę oraz przegląd ryzyk. Dla polskich organizacji to znaczy: warto ustandaryzować metodykę QRM, zadbać o to, żeby oceny były powtarzalne i wspierane danymi (trendami), a nie intuicją.
Outsourcing i nadzór nad partnerami jako element “state of control”
Polska jest mocna w usługach: CDMO, CMO, CRO, analityka, walidacje, pakowanie, dystrybucja. To świetnie, ale oznacza też, że temat umów jakościowych, odpowiedzialności, wymagań danych i reakcji na odchylenia jest kluczowy. W 2026 nie wystarczy, że “mamy podpisaną umowę”. Trzeba pokazać, że umowa działa: są przeglądy, są eskalacje, są audyty, są decyzje i zmiany.
W Polsce często jesteśmy świetni i postrzegani pod kątem “dowozimy produkcję”. A 2026 uczy, że musimy być równie dobrzy w “dowieźć dowody”, że produkcja jest pod kontrolą. Jedno bez drugiego w oczach FDA bywa połową historii.

