Dobry Validation Master Plan (VMP) to dokument definiujący podejście do walidacji jako całościowego systemu, a nie zbioru pojedynczych protokołów. Jak zauważył ISPE, VMP pełni rolę „mapy drogowej walidacji”, określającej kurs, strategię oraz działania zapewniające utrzymanie stanu zwalidowanego. Innymi słowy, VMP ma sprawić, że zespół walidacyjny i audytor wiedzą kto, co, dlaczego i w jakiej kolejności jest walidowane w zakładzie. Audytorzy nie są zainteresowani liczeniem protokołów, natomiast bardziej zależy im na tym, czy walidacja jest planowana, prowadzona i nadzorowana jako proces, oparty na ocenie ryzyka i z przypisanym odpowiednim, odpowiedzialnym personelem (zgodnie z duchem dojrzałego systemu jakości).
W niniejszym artykule przedstawiamy praktyczne wskazówki, jak zbudować VMP tak, aby:
- był zgodny z oczekiwaniami regulatorów i inspektorów (np. EU GMP Annex 15, Annex 11, FDA, wytycznymi ICH),
- ułatwiał codzienną pracę zespołu (logiczny i operacyjny charakter),
- mógł funkcjonować jako dokument „żywy” – podlegający aktualizacji i ciągłemu utrzymaniu.
Czym VMP jest, a czym nie jest
VMP to nadrzędny dokument zarządczy opisujący system kwalifikacji i walidacji w organizacji. Zawiera m.in.: politykę walidacji, zakres procesu, strategię i logikę ustalania priorytetów, role i odpowiedzialności, architekturę pakietów walidacyjnych (DQ/IQ/OQ/PQ itp.), sposób dokumentowania oraz mechanizmy utrzymania stanu zwalidowanego. W skrócie – to plan, który „nadaje ton” wszystkim działaniom walidacyjnym i zapewnia spójność (Annex 15 wymaga, aby kluczowe elementy programu walidacji były zdefiniowane i udokumentowane w VMP lub równoważnym dokumencie).
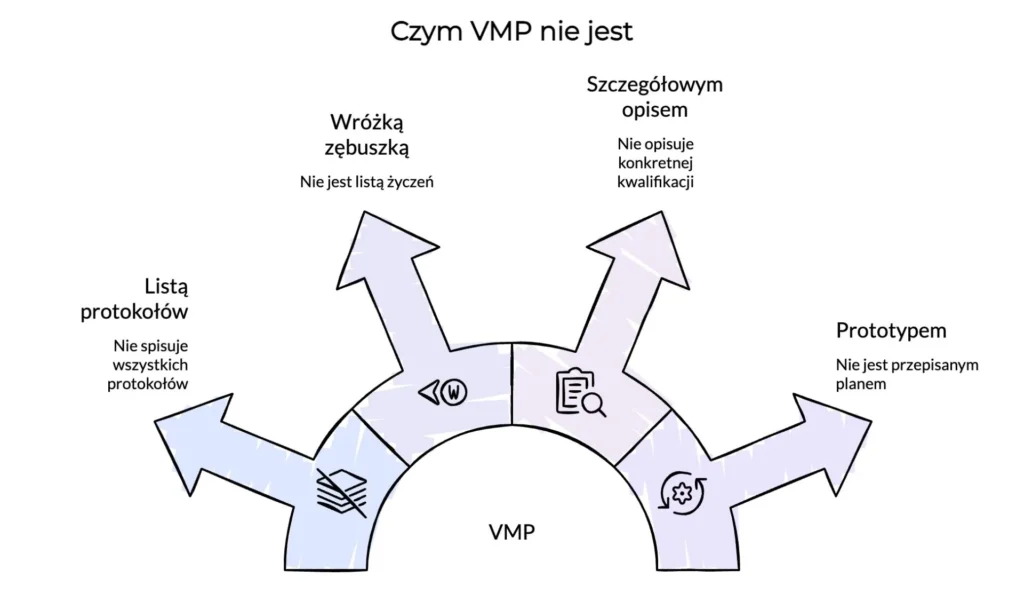
VMP nie jest:
- Asem dla kolekcjonera protokołów – nie stanowi spisu wszystkich protokołów walidacyjnych.
- Listą „życzeń”, o treści że „kiedyś wszystko zwalidujemy” (od tego jest np. lista statusu walidacji).
- Szczegółowym opisem jednej konkretnej kwalifikacji (do tego służą konkretne protokoły i raporty).
- Prototypem poprzedniego planu przepisanym bez uwzględnienia aktualnego obiektu i ryzyk.
Dobrze zaprojektowany VMP pozwala nowej osobie (lub audytorowi) od razu zrozumieć, kto w organizacji odpowiada za walidację, co i dlaczego jest walidowane, oraz według jakich zasad i kolejności są realizowane poszczególne działania.
Kiedy i co obejmuje VMP
Kiedy potrzebujemy VMP? W środowisku regulowanym aktualizacja lub opracowanie VMP jest zwykle konieczne przy każdym większym przedsięwzięciu, np.:
- uruchomienie nowego zakładu, linii produkcyjnej lub technologii,
- istotne zmiany w układzie pomieszczeń, systemach wentylacji, mediami krytycznymi lub systemach sterowania,
- wdrożenie/modernizacja systemów skomputeryzowanych (eQMS, eDMS, SCADA, MES itp.),
- przeniesienie procesu (transfer technologii) lub wprowadzenie istotnych zmian procesowych,
- potrzeba uporządkowania walidacji historycznej, która stała się nieprzejrzysta.
Zakres VMP zwykle obejmuje (lista orientacyjna):
- kwalifikację instalacji i infrastruktury (pomieszczenia, strefy, przepływy materiałów i personelu),
- kwalifikację sprzętu i urządzeń (DQ – specyfikacja projektowa, IQ – instalacja, OQ – działania funkcjonalne, PQ – wydajność w warunkach operacyjnych),
- kwalifikację mediów krytycznych (systemy HVAC, woda w procesach, gazy medyczne, sprężone powietrze itp.),
- walidację procesów technologicznych (planowaną zgodnie z cyklem życia procesu),
- walidację czyszczenia,
- walidację systemów skomputeryzowanych (CSV/CSA – zarówno aplikacji, jak i infrastruktury IT zgodnie z Annex 11),
- walidację metod analitycznych (o ile w organizacji leży razem z walidacją techniczną sprzętu laboratoryjnego),
- oraz „klej” łączący to wszystko: procedury zmian (change control), postępowanie z odchyleniami, przeglądy okresowe, rewalidacje czy szkolenia.
Oczekiwania regulacyjne
- EU GMP Annex 15: Wyraźnie wymaga, aby kluczowe elementy programu kwalifikacji i walidacji były zdefiniowane i udokumentowane w VMP lub równoważnym dokumencie. Annex 15 podaje też minimalny zestaw informacji, jakie VMP powinien zawierać – m.in. politykę walidacji, strukturę organizacyjną (role i odpowiedzialności) oraz podsumowanie obiektów/sprzętu objętych kwalifikacją.
- EU GMP Annex 11 (systemy komputerowe): Wymaga, by systemy skomputeryzowane były walidowane zgodnie z podejściem opartym na ocenie ryzyka. Annex 11 narzuca zasady integralności danych, bezpieczeństwa (kontrola dostępu, kopie zapasowe, przywracanie), ścieżek audytu oraz wymogi odnośnie elektronicznych zapisów i podpisów. Wymaga też ciągłego potwierdzania, że systemy działają poprawnie przez cały cykl życia i zgodnie z podejściem „risk-based”.
- FDA (walidacja procesów): Przewodnik „Process Validation: General Principles and Practices” akcentuje podejście opierające walidację procesów na cyklu życia produktu. Według FDA, lifecycle łączy rozwój procesu, jego kwalifikację oraz utrzymanie w kontroli podczas produkcji komercyjnej. W praktyce oznacza to, że walidacja nie kończy się na PPQ, lecz obejmuje ciągłe monitorowanie, zbieranie danych i weryfikację zdolności procesu.
- ICH Q9 (R1): Nowelizacja wytycznych Q9 podkreśla rolę systematycznej oceny ryzyka, przy czym zwraca szczególną uwagę na niebezpieczeństwo subiektywności w ocenie. Innymi słowy, analiza ryzyka powinna być przeprowadzona w sposób przejrzysty, zdefiniowany i możliwy do obrony przed audytorem.
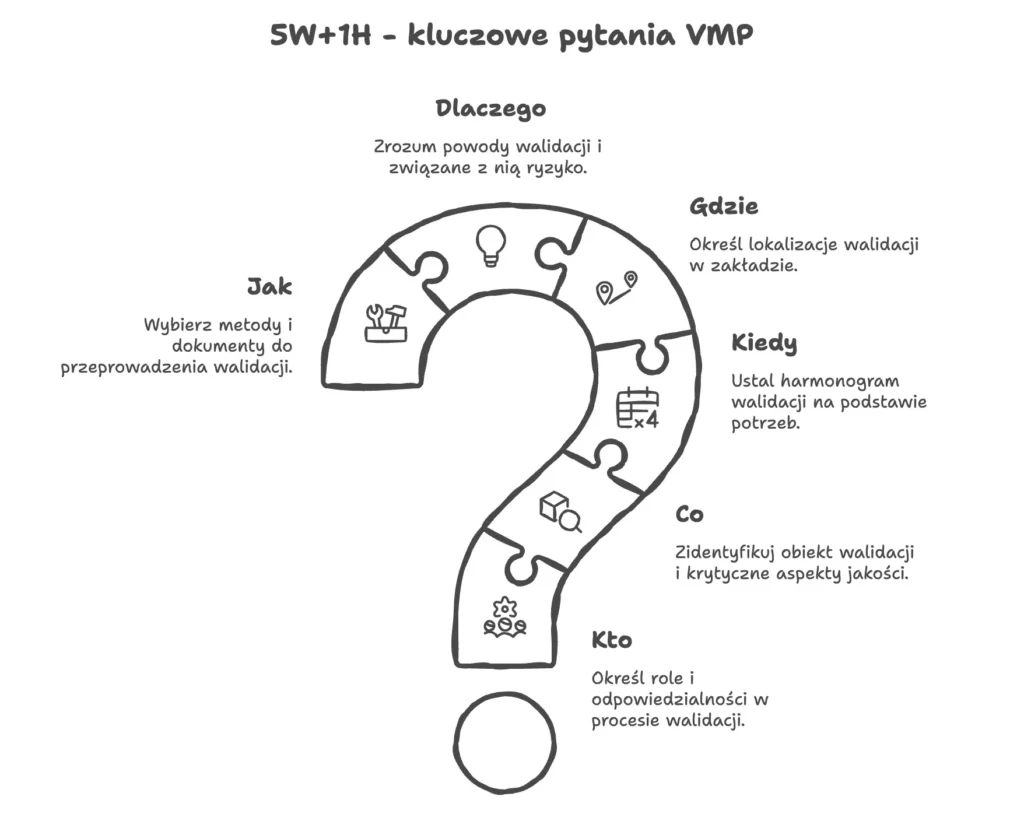
Zasada 5W+1H – kluczowe pytania VMP
Aby VMP był czytelny i kompletny, powinien w prosty sposób odpowiedzieć na sześć podstawowych pytań:
- Who (kto): Kto jest właścicielem walidacji (Process/Validation Owner)? Kto opracowuje dokumentację (URS, protokoły)? Kto zatwierdza protokoły i raporty? Kto odpowiada za nadzór jakości (QA)?
- What (co): Co jest obiektem walidacji? Co uznajemy za krytyczne z punktu widzenia jakości/bezpieczeństwa (a co nie wymaga walidacji)?
- When (kiedy): Kiedy walidację się przeprowadza – czy są to nowe instalacje, istotne zmiany, rutynowe rekwalifikacje, okresowe przeglądy? Kiedy uruchamiamy poszczególne pakiety walidacyjne?
- Where (gdzie): Gdzie odbywa się walidacja – jakie pomieszczenia, strefy lub lokalizacje zakładu obejmuje (np. produkcja, magazyn, QC)?
- Why (po co): Dlaczego dana walidacja jest potrzebna – jakie ryzyko na jakość produktu, bezpieczeństwo pacjenta/użytkownika lub integralność danych się z nią wiąże?
- How (jak): Jakie metody, standardy i dokumenty stosujemy? W jaki sposób definiujemy akceptowalne kryteria, jak prowadzimy testy, oraz jak zarządzamy odchyleniami i zmianami?
Jeśli VMP nie odpowiada na te pytania w sposób spójny, to zespół walidacyjny będzie musiał improwizować „w trakcie walki” – co niemal zawsze prowadzi do niespójności i nieefektywności w późniejszym etapie.
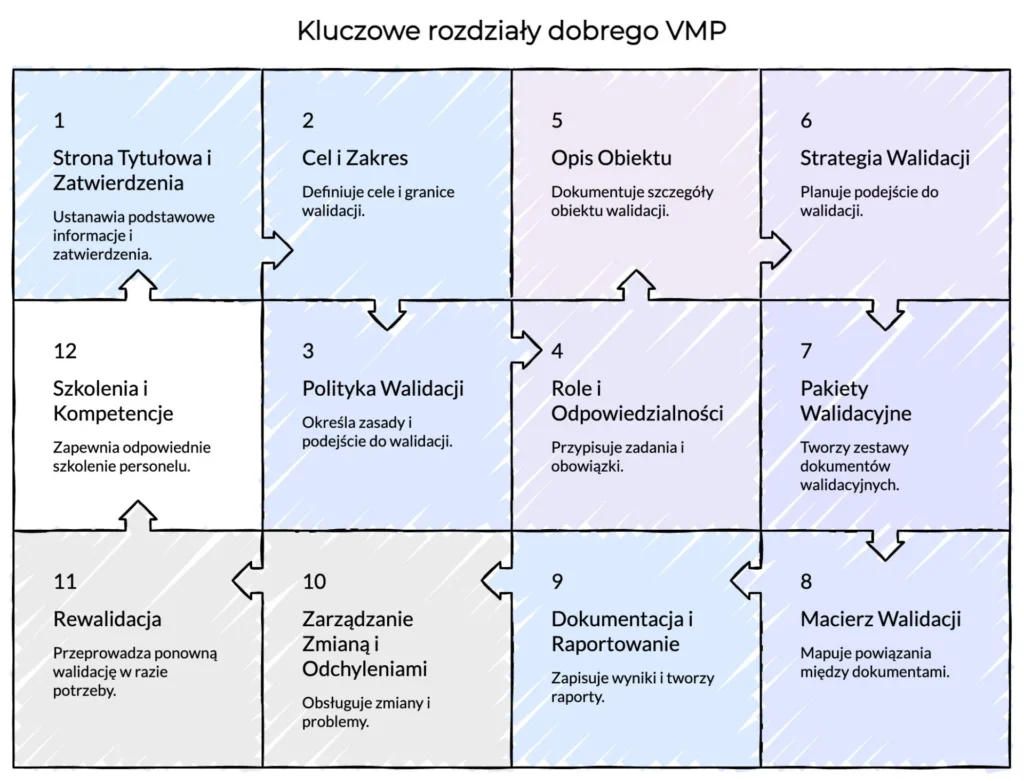
Kluczowe rozdziały dobrego VMP
Poniżej podsumowujemy najważniejsze sekcje, które powinien zawierać dobrze przygotowany VMP, wraz z praktycznymi wskazówkami:
1. Strona tytułowa, wersjonowanie, zatwierdzenia
- Wyraźnie wskaż numer dokumentu, wersję i datę wejścia w życie.
- Określ właściciela dokumentu (np. Validation Owner) oraz wymagane podpisy zatwierdzające (szczególnie nadzór jakości, który powinien aktywnie uczestniczyć w walidacji).
- Zamieść historię zmian: krótki opis, co zostało zmienione i dlaczego.
- Wskazówka: Jeśli organizacja ma problem z „martwymi dokumentami”, w VMP warto ustalić twardy harmonogram przeglądów (np. roczny) i procedurę inicjowania aktualizacji.
2. Cel, zakres i definicje
- Krótko opisz, czym jest walidacja w kontekście organizacji (np. zdefiniuj terminy „walidacja”, „kwalifikacja”, „stan zwalidowany”).
- Określ, jaki obszar organizacji obejmuje dokument (zakład, lokalizacje, określone linie produkcyjne lub procesy).
- Wylicz, co jest w zakresie walidacji, a co wyłączone (i uzasadnij wyłączenia – każde „puste pole” w systemie walidacji wygląda jak luka, jeśli nie ma do tego logicznego wytłumaczenia).
- Wskaż, jak VMP wpisuje się w ogólny system jakości (np. jest częścią Szerszej Polityki Jakości/Quality Manual) i do jakich dokumentów się odnosi (np. standardowe procedury operacyjne – SOP-y, dokumenty specyfikacji itp.).
3. Polityka walidacji i podejście lifecycle
- Opisz filozofię: walidacja to proces obejmujący cały cykl życia instalacji/procesu, a nie jednorazowe „zdarzenie”. Zgodnie z Annex 15 i podejściem FDA, walidacja powinna być zorganizowana tak, aby odzwierciedlać projektowanie procesu, jego kwalifikację i utrzymanie w kontroli.
- Uwzględnij podejście oparte na ocenie ryzyka (risk-based planning). Wyjaśnij, jak definiujesz „ryzyko” (jako wpływ na jakość/bezpieczeństwo) oraz jakie kryteria decydują o konieczności poszczególnych działań walidacyjnych.
- Opisz zasady kwalifikacji sprzętu (DQ, IQ, OQ, PQ): kiedy stosujemy każdy etap i jakie stawiamy standardy.
- Uwzględnij zasady walidacji procesów: np. model 3-fazowy (projektowanie, kwalifikacja, weryfikacja ciągła) czy liczbę serii walidacyjnych w oparciu o ryzyko.
- Określ podejście do rekwalifikacji/rewalidacji: jakie są triggery (np. zmiana wyposażenia, parametrów, materiałów, dostawców) i jakie procedury przeglądów okresowych (np. corocznych) będą stosowane.
4. Role i odpowiedzialności
- Zamiast ogólników typu „QA nadzoruje jakość”, dokładnie wymień, kto konkretnie odpowiada za poszczególne zadania:
- kto formułuje wymagania użytkownika (URS) i specyfikacje,
- kto opracowuje i zatwierdza protokoły DQ/IQ/OQ/PQ,
- kto ocenia i akceptuje wyniki oraz ewentualne odchylenia,
- kto utrzymuje raport w stanie zwalidowanym po zakończeniu projektu,
- kto inicjuje ocenę zmian i prowadzi proces change control,
- kto jest odpowiedzialny za przeglądy okresowe i nadzór.
- Jeśli zachodzi ryzyko konfliktu kompetencji (np. granica między QA a działem utrzymania ruchu, między produkcją a walidacją, między IT a biznesem), opisz mechanizmy ich rozstrzygania (np. komitet walidacyjny, nadzorujący audytów wewnętrznych).
- Upewnij się, że do żadnej kluczowej funkcji walidacyjnej nie pozostaje „brak przypisanego właściciela” – to częsty błąd, który warto wyeliminować już na etapie planu.
5. Opis obiektu (facility description)
- VMP powinien zawierać zwięzły opis obiektu i jego głównych komponentów, ponieważ walidacja dotyczy konkretnej infrastruktury, a nie abstrakcyjnego urządzenia. Opisz:
- ogólny układ zakładu i główne przepływy (surowców, personelu, produktów),
- strefowania (jeśli obowiązują), śluzy i granice krytyczne między strefami,
- główne obszary operacyjne (produkcja, magazyny, laboratorium QC, strefy wsparcia itp.),
- wykaz kluczowych systemów i mediów krytycznych (np. HVAC, woda procesowa, sprężone powietrze, gazy techniczne).
- Celem nie jest tworzenie atlasu technicznego, ale przedstawienie kontekstu potrzebnego do zrozumienia logiki planu walidacji. Annex 15 wymaga podsumowania obiektów, systemów i procesów objętych kwalifikacją, więc warto tu zawrzeć przegląd tych elementów oraz ich bieżący status kwalifikacji/walidacji.
6. Strategia walidacji oparta na ocenie ryzyka
- Opisz, jak organizacja podchodzi do oceny ryzyka w walidacji. Wskaż:
- kryteria ryzyka – na jakie aspekty patrzymy (np. wpływ na jakość produktu, bezpieczeństwo pacjenta/użytkownika, integralność danych),
- narzędzia oceny ryzyka – FMEA, matryce ryzyka, HACCP itp. (bez przywiązywania się dogmatycznie do jednego narzędzia),
- ograniczenie subiektywności – ICH Q9(R1) podkreśla konieczność nadzoru nad subiektywnością w ocenie ryzyka. W VMP warto opisać, jak ustalamy definicje prawdopodobieństwa i skutku, aby analiza była spójna i powtarzalna.
- Wskazówka praktyczna: Przeprowadź warsztaty QRM z jasnym wprowadzeniem (ustaleniem skali ocen i definicji) – inaczej „rachunek emocji” wprowadzi niepotrzebne rozbieżności. Dobrze przeprowadzona ocena ryzyka będzie realnie wpływać na zakres i częstotliwość walidacji (np. mniejszy zakres testów przy niskim ryzyku, szybsza rewalidacja przy wykrytych problemach).
7. Pakiety walidacyjne (DQ/IQ/OQ/PQ, CSV itp.)
Podział na strumienie walidacyjne: W praktyce VMP dzieli pakiety walidacyjne na główne obszary, ponieważ każdy ma inne wymagania, dokumenty i ryzyka. Typowe kategorie to:
- a) Kwalifikacja wyposażenia i instalacji (DQ/IQ/OQ/PQ):
- DQ (Design Qualification): definiowanie wymagań użytkownika (URS) i kryteriów projektowych sprzętu. W VMP opisz, jak łączyć DQ z wymaganiami biznesowymi i URS.
- IQ (Installation Qualification): potwierdzanie zgodności instalacji (mechanika, elektryka, automatyka) ze specyfikacją.
- OQ (Operational Qualification): testowanie funkcji urządzenia w pełnym zakresie warunków operacyjnych.
- PQ (Performance Qualification): ocena powtarzalności i jakości działania w normalnym cyklu produkcyjnym.
- Standardy i raporty: Określ organizacyjne standardy dla protokołów i raportów końcowych – np. jak wygląda zatwierdzanie, ocena odchyleń, struktura dokumentów. Dzięki temu każdy protokół będzie spójny w całej firmie.
- b) Kwalifikacja mediów krytycznych (HVAC, woda, gazy):
- Wymień kluczowe parametry każdego medium (np. temperatura, ciśnienie, jakość wody, czystość powietrza).
- Opisz plan monitoringu i okresy pomiarów.
- Pokaż, jak walidacja łączy się z utrzymaniem: harmonogramy przeglądów, kalibracje przyrządów pomiarowych, analizowanie trendów danych w czasie. Audytor szczególnie przygląda się media systemom jako potencjalnym źródłu zanieczyszczeń, więc jasność tych ustaleń jest kluczowa.
- c) Walidacja procesów (Process Validation – lifecycle):
- Obejmuje wybór procesów do walidacji, definiowanie krytycznych parametrów/atrybutów (CPP/CQA) i planowanie testów.
- Zgodnie z podejściem lifecycle (FDA) proces waliduje się etapowo: projekt (zgodnie z wiedzą z rozwoju), kwalifikacja (potwierdzenie reprodukowalności procesu) i stała weryfikacja (monitoring produkcji).
- W VMP opisz, jak określasz liczbę wsadów walidacyjnych oraz dlaczego jest ona wystarczająca, a także jak prowadzisz Continued Process Verification (ciągłą weryfikację) podczas produkcji komercyjnej (monitoring danych, analiza trendów, okresowe przeglądy).
- d) Walidacja czyszczenia:
- Określ sposób grupowania sprzętu do walidacji (podejście worst-case, np. różne technologie procesowe).
- Wskaż, które substancje zabrudzeń przyjmujesz za referencyjne.
- Opisz, jak ustalasz limity dopuszczalnego zanieczyszczenia oraz metody poboru próbek (gdzie i jak często pobierasz próbki do analizy).
- Wyjaśnij sposób postępowania ze zmianami (np. nowy detergent lub zmiana konfiguracji maszyny): jakie są procedury ponownego przeglądu i walidacji po zmianie.
- e) Walidacja systemów skomputeryzowanych (CSV/CSA) i integralność danych:
- Zidentyfikuj systemy podlegające walidacji, zgodnie z wpływem GxP.
- W VMP opisz, jak definiujesz wymagania (URS) dla systemów i jak planujesz testy (plany testów, skrypty testowe).
- Uwzględnij rolę dostawców (np. w GAMP5 przewodniku) – ich dokumentację, wsparcie w testach i audyty u dostawcy.
- Podkreśl rozwiązania zapewniające integralność danych: zgodnie z Annex 11 dane muszą być dokładne, kompletne i spójne przez cały cykl życia, dlatego VMP powinien opisać zarządzanie uprawnieniami, ścieżki audytu, backupy i procedury przywracania, a także kontrolę zmian systemów.
- f) Walidacja metod analitycznych (jeśli w tym samym zakresie):
- Opisz, kiedy stosować pełną walidację metody (np. przy wdrażaniu nowej metody), a kiedy wystarczy weryfikacja lub transfer metody.
- Wskaż, jak zmiany w metodach są kontrolowane (np. ponowna walidacja po zmianie warunków analitycznych).
- Jeśli jest to część tego samego systemu, połącz kwestię walidacji metod z kwalifikacją aparatury laboratoryjnej (urządzenia wykonujące analizy powinny być odpowiednio zwalidowane/skalibrowane).
8. Macierz walidacji i powiązania dokumentacyjne (traceability)
- Utrzymuj macierz walidacji (traceability matrix), która łączy wymagania (URS/specyfikacje) z przeprowadzonymi testami (protokoły) i wynikami (raporty walidacyjne).
- W VMP opisz, jak ta macierz jest tworzona i aktualizowana – np. czy korzystacie z narzędzia (eQMS) czy z arkusza kalkulacyjnego. W przypadku systemowego zarządzania matryca jest ciągłym mechanizmem śledzenia, co audytor doceni jako element sterowania procesem. Jeśli jest to pojedynczy Excel, warto to również jasno zaznaczyć jako tymczasowe rozwiązanie.
- Cel macierzy: szybkie udowodnienie inspekcji „co walidowaliśmy dla tego systemu i gdzie znajduje się dowód”. Dzięki niej unikamy sytuacji, że każdy protokół wygląda inaczej – wszystko jest spójnie powiązane.
9. Dokumentacja i raportowanie
- Annex 15 wymaga, aby VMP odwoływał się do obowiązujących zasad dokumentacji i akceptacji wyników. W tej sekcji należy więc przedstawić:
- używane szablony protokołów i raportów (np. format URS, IQ, OQ, PQ),
- strukturę raportów końcowych i kryteria ich akceptacji (kto i w jakim trybie zatwierdza raport podsumowujący walidację),
- procedurę postępowania z odchyleniami (klasyfikacja odchylenia, jego wpływ na stan zwalidowany, dokumentacja decyzji).
- Uporządkowanie standardów dokumentacyjnych w VMP zapobiega „chaosowi formatów” – każdy protokół i raport powinien być tworzony według tych samych zasad, co znacznie przyspiesza przygotowanie dokumentacji i jej ocenę przez audytora.
10. Zarządzanie zmianą, odchyleniami i rewalidacją
- Opisz, jak change control ocenia wpływ każdej zmiany na dotychczasowy stan zwalidowany.
- Wskaż typowe triggery rekwalifikacji/rewalidacji: np. istotne modyfikacje sprzętu, zmianę parametrów procesowych, aktualizację oprogramowania czy zmianę krytycznych dostawców.
- Podkreśl obowiązek okresowych przeglądów („periodic review”) – np. coroczne przeglądy dla kluczowych systemów – wraz z mechanizmem uwzględniania trendów monitoringu.
- Warto pamiętać: Organizacje zwykle nie przegrywają audytów dlatego, że nie wykonały IQ, a raczej dlatego, że nie potrafią wykazać, iż po wprowadzeniu zmian i po serii odchyleń proces nadal jest kontrolowany. VMP musi to uwzględniać, nakreślając sposób dokumentowania wpływu odchyleń i zmian na walidację.
Uwaga: zarządzanie zmianą w ramach walidacji zawsze rekomendujemy prowadzić w ramach podsystemu. Zarządzanie zmianą w globalnym systemie w dużej organizacji może znacznie spowolnić reakcje na zmiany, które w walidacji często wymagają szybkiego działania.
11. Szkolenia i kompetencje
- Annex 15 podkreśla, że działania walidacyjne powinny być wykonywane przez osoby odpowiednio wykwalifikowane. W VMP nie ma potrzeby zamieszczać całej matrycy szkoleń, ale warto wskazać:
- jakie kompetencje (specjalistyczna wiedza, certyfikaty, doświadczenie) są wymagane na kluczowych stanowiskach walidacyjnych,
- jak weryfikujemy, że dana osoba jest gotowa do przeprowadzenia walidacji (np. ocena efektywności szkoleń, zatwierdzanie przez przełożonego),
- jak szkolimy z procedur postępowania z odchyleniami, zasad change control i innych procesów walidacyjnych (często pod presją terminów takie umiejętności wypadają z głowy).
- Dzięki temu VMP potwierdza przed audytorami, że personel zaangażowany w walidację dysponuje niezbędną wiedzą i doświadczeniem.
Priorytety i realistyczne planowanie
W praktyce nie da się walidować wszystkiego naraz. Priorytety projektu walidacji powinny wynikać z oceny trzech osi:
- Wpływ na jakość/bezpieczeństwo/integralność danych,
- złożoność techniczna i podatność na awarie,
- historia problemów (odchylenia, reklamacje, obserwacje z poprzednich inspekcji).
To jak z remontem: możesz najpierw wymienić klamki (element estetyczny), ale jeśli instalacja elektryczna iskrzy, to to właśnie powinno być priorytetem. VMP powinien odzwierciedlać tę logikę – skupienie na najbardziej krytycznych aspektach walidacji (risk-based prioritization) zamiast realizacji wszystkich zadań w jednej kolejności.
Najczęstsze błędy i jak ich unikać
- Zbyt ogólny VMP („podręcznik walidacji”): Nie dopasowany do specyfiki obiektu. Remedium: Dodaj dokładny opis obiektu i systemów, uzasadnij wybór zakresu walidacji analizą ryzyka, dołącz macierz walidacji.
- Brak przypisanego właściciela po zakończeniu projektu: VMP powinien jasno wskazywać, kto utrzymuje stan zwalidowany, prowadzi przeglądy okresowe i reaguje na zmiany. Remedium: Przypisz odpowiedzialność za utrzymanie walidacji (np. „Validation Steward”), wraz z planem nadzoru i procedurą change control.
- Analiza ryzyka „dla formalności”: Ocena ryzyka nie wpływa na rzeczywisty zakres testów ani harmonogramu. Remedium: Pokaż, że ryzyko steruje zakresem testów i harmonogramem (np. mniej testów tam, gdzie ryzyko jest niskie). Wprowadź zasady ograniczania subiektywności oceny (patrz ICH Q9(R1)), aby wyniki były powtarzalne i uzasadnione.
- Harmonogram „życzeniowy”: Nie uwzględnia zasobów, czasu na obsługę odchyleń, opóźnień dostaw. Remedium: Buduj harmonogram z realnym buforem czasowym, określ kluczowe punkty decyzyjne (go/no-go) i uwzględnij czas na poprawki.
FAQ
- Czym VMP różni się od protokołów walidacyjnych? VMP to dokument strategiczny opisujący system zarządzania walidacją (polityki, zakres, role, logikę). Protokoły walidacyjne to szczegółowe instrukcje wykonania testów dla konkretnego urządzenia lub procesu, zakończone raportem. VMP nie zawiera treści testów – pokazuje tylko ich ramy i zasadność.
- Czy VMP może obejmować kilka obiektów lub projektów? Może, jeśli jest to czytelnie zorganizowane (np. wspólna część polityki i załączniki specyficzne dla każdego obiektu). Wiele obiektów jednym planem wymaga wyraźnego podziału (np. osobne tabele, matryce i harmonogramy). Annex 15 sugeruje wręcz, że dla skomplikowanych projektów osobne VMP mogą zwiększyć przejrzystość.
- Czy VMP można zmieniać po zatwierdzeniu? Tak. VMP powinien być dokumentem „żywym” – aktualizowany w oparciu o change control. Każda zmiana musi być uzasadniona, zatwierdzona i oceniona pod kątem wpływu na walidację.
- Jak szczegółowy powinien być VMP? Na tyle, by efektywnie zarządzać walidacją i uzasadnić logikę przed audytorem, ale nie tak szczegółowo, żeby w nim znalazły się testy protokołów. Szczegółowe procedury i testy pozostaw protokołom i SOP-om.
Podsumowanie
Validation Master Plan to nie kolejna kartka do segregatora, lecz dokument scalający walidację w jeden sterowalny system – od oceny ryzyka, przez strategię i procedury, aż po dowody i utrzymanie zwalidowanego stanu. Dobry VMP sprawia, że audytor widzi spójny proces walidacyjny, a zespół pracuje zgodnie z ustalonymi zasadami. Złe przygotowanie VMP przekłada się na chaos i wiele nerwów podczas inspekcji – dlatego warto poświęcić czas na jego solidne opracowanie.
Jak możemy pomóc (CTA)
Jeśli potrzebujesz wsparcia przy VMP, oferujemy działania na trzech poziomach:
- Konsultacja 1:1 – Przeanalizujemy wraz z Tobą zakres walidacji, zidentyfikujemy kluczowe ryzyka i ocenimy gotowość organizacji. Pomagamy dobrać odpowiednią strategię VMP dopasowaną do konkretnego obiektu i produktów.
- Opracowanie VMP end-to-end – Przygotujemy kompletny dokument VMP, od polityki walidacji po szczegółową matrycę i governance. Uwzględnimy pakiety walidacyjne, schemat organizacyjny oraz mechanizmy utrzymania walidacji w czasie.
- Szkolenie zespołu (QA/Engineering/IT/Production) – Przeprowadzimy warsztaty i szkolenia, aby VMP nie był „dokumentem konsultanta”, lecz wspólnym standardem pracy. Zespół pozna w nich nasze praktyki QRM, mechanizmy change control i zasady efektywnej walidacji, dzięki czemu łatwiej będzie utrzymać VMP w życiu i obronić go przed audytorami.

